Open INESEM
Investigación

Ensayo clínico sobre la eficacia de Faimerol en el tratamiento de la enfermedad de Alzheimer
1. Introducción
La enfermedad de Alzheimer (EA) es una enfermedad neurodegenerativa que representa el 60-70% de los casos de demencia (Scheltens et al. 2016). Su incidencia en Europa es del 11,8 por 1000 personas por año, dato que asciende de forma exponencial a partir de los 65 años, y con una prevalencia en Europa del 5% y en España del 6% entre los 60-65 años (Niu et al. 2017; Garre-Olmo 2018). La EA fue descrita por primera vez en 1906 por Alois Alzheimer y se caracteriza por una pérdida neuronal en distintas regiones cerebrales, como la corteza entorrinal, el hipocampo y la corteza cerebral (Hippius & Neundorfer 2003).
Los síntomas clínicos de esta enfermedad engloban los 8 dominios intelectuales: la memoria, el lenguaje, las capacidades relacionadas con la percepción, la atención, las habilidades motoras y de orientación, la capacidad de resolución de problemas y las funciones ejecutivas; apareciendo en estadios avanzados pérdida de recuerdos de la memoria consolidada, alteraciones en el lenguaje, desorientación, cambios bruscos de humor, incapacidad de autocuidado y alteraciones del comportamiento y psicológicas (agresividad, psicosis…) (Scheltens et al. 2016; Ower et al. 2018).
Con respecto a las alteraciones neuropatologías relacionados con la EA, las más destacadas son: la formación de depósitos de la proteína beta-amiloide (placas seniles), la acumulación de tau hiperfosforilada (ovillos neurofibrilares), el descenso de la acetilcolina, la excitotoxicidad promovida por glutamato, la alteración en la transmisión sináptica y la neuroinflamación (Burns and Iliffe 2009; Panza et al. 2016; Selkoe & Hardy 2016).
La EA es una demencia multifactorial y heterogénea que engloba diferentes etiologías (mecanismos etiopatogénicos), pudiendo ser origen genético o esporádico (Ballard et al. 2011; Hardy et al. 2014). La EA familiar o de origen genético (1% de los casos) se desarrolla debido a mutaciones en la proteína precursora del péptido β-amiloide (APP), en la presenilina 1 (PS1) o 2 (PS2) (Méndez 2012; Bagyinszky et al. 2014). Mientras que la EA esporádica engloba la mayoría de casos de EA y parece desarrollarse debido a un conjunto de factores genéticos y ambientales, entre los que se encuentran: diversas alteraciones metabólicas (hipercolesterolemia e hiperglucemia), la hipertensión arterial, el daño vascular, el consumo de tabaco, el déficit en diversas vitaminas, el estrés psicológico, los cambios en la microbiota intestinal e infecciones periodontales crónicas y las mutaciones en la apolipoproteína E4, entre otros factores (Rosendorff et al. 2007; Cataldo et al. 2010; Anstey et al. 2011; Guerreiro & Hardy 2014).
El diagnóstico de los pacientes de EA se realiza mediante test cognitivos, resonancias magnéticas y medición de ciertos marcadores en sangre y/o líquido cefalorraquídeo. El NIA-AA (National Institute on Aging-Alzheimer's Association and the Alzheimer’s Association) criteria es el criterio de diagnóstico más usado (McKhann et al., 2011). Este criterio tiene en cuenta los 8 dominios intelectuales que se ven alterados en la EA, recopilados en el DSM-IV (Diagnostic and Statistical Manual of Mental Disorders), y analiza las alteraciones cognitivas mediante test neuropsicológicos, como el MMSE (Mini-Mental State Examination) (Folstein et al., 1975). También tiene en cuenta la expresión de diversos biomarcadores para obtener un diagnóstico clínico de posible o probable caso de EA. En cuanto a la evaluación neuropatológica de la enfermedad, que se realizará postmortem, se siguen los criterios de la guía del NIA-AA (Hyman et al., 2012).
El interés por encontrar un tratamiento efectivo para la EA ha sido acuciante en los últimos años (Ballard et al. 2011; Anand et al. 2014; Cummings et al. 2019). Según los datos del clinicaltrial.gov, hasta la fecha se han realizado más de 2000 estudios clínicos para esta enfermedad, más de 140 de ellos en España (17 de ellos en activo). Por otro lado, en el Registro Español de ensayos clínicos (REec) aparecen bajo el criterio de búsqueda de “enfermedad de Alzheimer” 90 estudios inscritos, 55 de ellos finalizados.
Los fármacos que han sido o están siendo testados en ensayos clínicos de EA tienen como diana los 5 puntos clave, conocidos hasta la fecha, implicados en el desarrollo de la EA (Hung & Fu 2017; Moussa 2017; Cummings et al. 2019): los niveles de acetilcolina, los depósitos de beta-amiloide, la fosforilación y acumulación de tau, y la excitotoxidad y los procesos neuroinflamatorios.
Entre los fármacos autorizados para el tratamiento de la EA se encuentran los anticolinesterásicos donepezilo, galantamina y rivastigmina; y el bloqueante de la transmisión glutamatérgica memantina (Thomas & Grossberg 2009). El último de estos fármacos fue aprobado por la FDA (Food and Drugs Administration) en 2003. Estos fármacos tienen un efecto paliativo, pero no curativo sobre esta enfermedad; y ninguno de los fármacos testados hasta el momento ha demostrado un efecto curativo en la EA, evidenciando la necesidad de encontrar nuevas estrategias terapéuticas para el tratamiento de la EA.
El fármaco Faimerol
La proteína FAIME se ha postulado como una posible diana terapéutica para el tratamiento de la EA debido a sus importantes funciones en el sistema nervioso central, su papel en la modulación de los niveles de la proteína tau, el descenso de la expresión de FAIME en distintas regiones cerebrales en pacientes con EA, y la mejora cognitiva observada en modelos de EA tras su sobreexpresión.
Por ello, se decidió desarrollar un peptidomimético de la proteína FAIME. La ventaja que confiere el uso de un fármaco peptidomimético es la posibilidad de modificar su biodisponibilidad y farmacocinética. El compuesto resultante de años de estudio en la materia fue Faimerol. La seguridad/toxicidad y eficacia del fármaco fue testada en ensayos preclínicos siguiendo las directrices de las buenas prácticas de producción y los criterios pautados por la Conferencia Internacional para la Armonización de los Requisitos Técnicos para el Registro de Productos Farmacéuticos para Uso Humano (International Conference on Harmonisation 2009).
Los resultados del estudio preclínico mostraron la dosis efectiva y máxima tolerada de Faimerol, su farmacodinamia y farmacocinética, y confirmaron la seguridad del fármaco para su uso en ensayos clínicos; al no observarse afectación de la función respiratoria, cardiovascular o nerviosa en los organismos testados.
Tras la aprobación del ensayo preclínico por las Autoridades Competentes se iniciaron los ensayos clínicos de Fase I (estudio aleatorio, en paralelo, con dosis creciente del fármaco) con el fármaco Faimerol. Estos ensayos determinaron la seguridad y tolerabilidad de este fármaco establecido la dosis terapéutica (60mg) y la dosis máxima tolerada en humanos (120 mg). En este punto, Faimerol, un peptidomimético de la proteína FAIME capaz de atravesar la BHE y de administrarse por vía oral se muestra como un interesante candidato para evaluar su eficacia en el tratamiento de la EA.
2. Sinopsis del Protocolo del Ensayo Clínico
2.1. Objetivos del ensayo
Objetivo principal: evaluar la eficacia de Faimerol a dos dosis de tratamiento en la enfermedad de Alzheimer.
Objetivos secundarios:
a) Confirmar la seguridad de Faimerol en los sujetos del estudio y
b) Determinar sus parámetros farmacocinéticos en la población de estudio.
2.2. Diseño y descripción del ensayo
Es un ensayo clínico de fase II cerrado, aleatorizado, controlado por placebo, triple ciego, paralelo, con análisis por intención de tratar; que busca valorar la eficacia y seguridad del fármaco Faimerol administrado durante 50 semanas de forma oral en pacientes con EA leve en 3 brazos experimentales.
El seguimiento y valoración del efecto de la intervención terapéutica, administración oral de Faimerol a dos dosis potencialmente seguras (60 y 12 mg), se realizarán a lo largo de 52 semanas. Se llevarán a cabo las visitas pertinentes a las semanas 4, 16, 24 y 32 tras el inicio del tratamiento y 2 semanas tras el cese del tratamiento.
Los pacientes del estudio serán seleccionados siguiendo los criterios de inclusión y exclusión que serán descritos posteriormente, previo consentimiento informado antes de la inclusión en el estudio.
Los participantes del estudio serán asignados mediante aleatorización por bloques balanceados a uno de los brazos del ensayo clínico, asignándose el número correspondiente en base a los criterios del estudio. El tratamiento asignado permanecerá enmascarado para el participante del estudio, el investigador y el personal asignado para el análisis de los datos a menos que se requiera un desenmascaramiento del estudio para asegurar el bienestar de los sujetos de estudio. Una vez efectuada la aleatorización se realizará la visita de screening que incluirá una resonancia magnética (RM), análisis bioquímicos y una batería de test cognitivos.
En las visitas posteriores, 4, 16, 24, 32 semanas tras el inicio del tratamiento, se realizarán diversos test cognitivos siguiendo el esquema de la figura 1. En la última visita, 2 semanas tras el cese del tratamiento (semana 52) se realizará una batería de test cognitivos (COWAT, test de los dígitos, test de comprensión oral y test de la fluidez verbal), evaluación de biomarcadores en sangre y LCR y una RM a tiempo final.
La presencia de acontecimientos adversos/acontecimientos adversos graves en los participantes del estudio se reportará en cualquier momento del estudio, incluyendo las 50 semanas de tratamiento y las 2 semanas tras el cese del tratamiento.
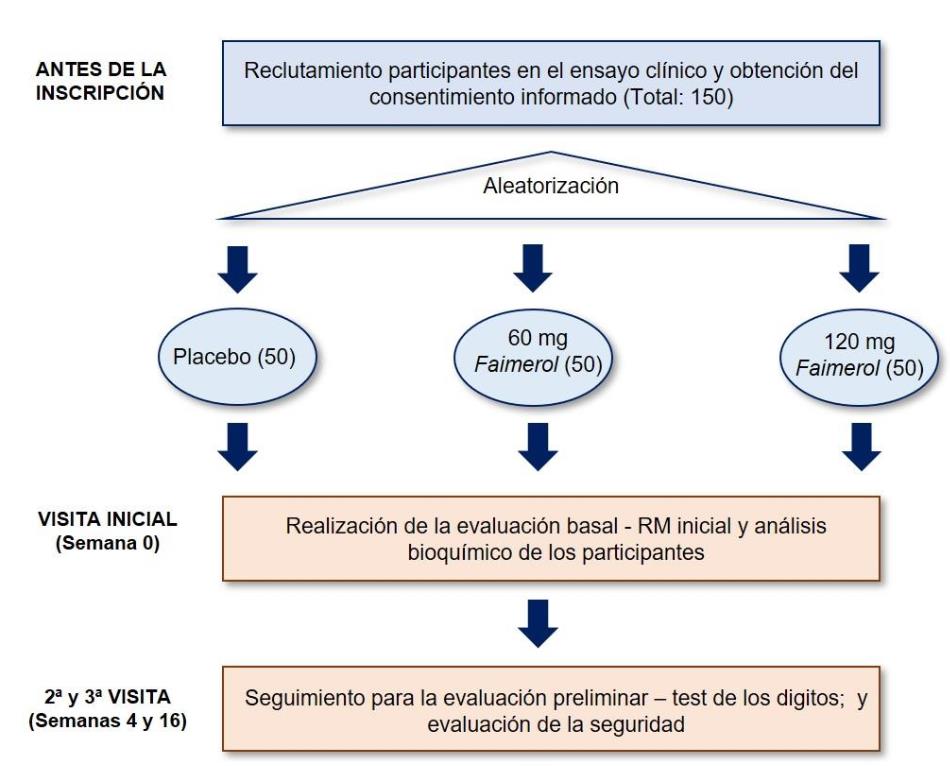
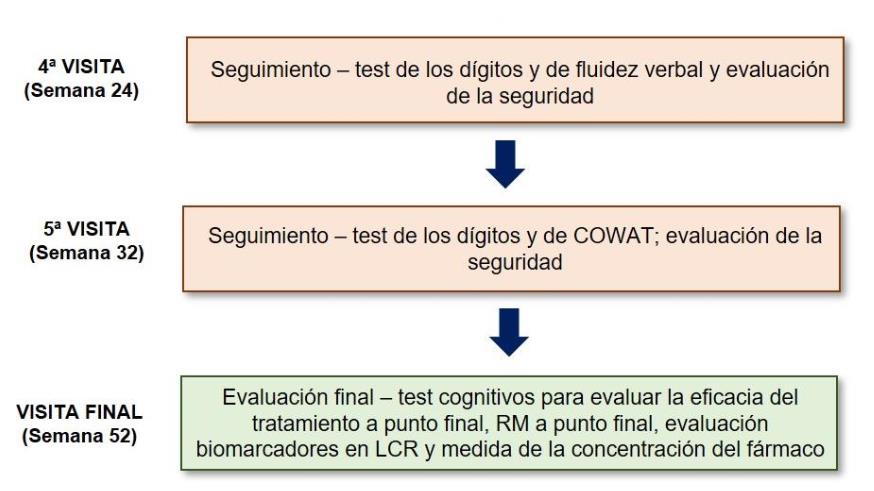
Figura 1. Procedimiento general del ensayo clínico
2.3. Población de estudio
La población de estudio incluirá a pacientes de ambos sexos, con edades comprendidas entre 60 y 80 años que cumplan con los criterios de selección y no presenten ningún criterio de exclusión preestablecido. El tamaño muestral será de 150 sujetos (50 por condición) y los brazos experimentales serán aleatorios por bloques balanceados, a los grupos 60 mg de Faimerol, 120 mg de Faimerol y placebo (50 pacientes por condición).
2.4. Criterios de inclusión y exclusión
Criterios de inclusión:
- Consentimiento informado para participar en el estudio.
- Hombres y mujeres entre 60-80 años. - Las mujeres participantes deben usar métodos para evitar la concepción o encontrarse en período no fértil.
- Diagnóstico de posible o probable enfermedad de Alzheimer de acuerdo con el criterio NIA-AA (Mckhann 2011) en estadio leve, valores comprendidos entre 25-20 en el MMSE.
- Los pacientes viven con un familiar como principal cuidador o un cuidador profesional que puede acompañarlos a todas las intervenciones y consultas de seguimiento o están capacitados para acudir a las visitas por ellos mismos.
- El paciente no presenta déficits sensoriales en los estudios previos.
- El sujeto tiene habilidad para tragar pastillas.
- En el caso que reciba un tratamiento para la EA, éste sea un tratamiento convencional para dicha enfermedad de forma estable, es decir, el tratamiento no ha sufrido modificaciones al menos en los últimos 90 días antes su selección para este ensayo clínico.
- Si el paciente recibe medicación para enfermedades comórbidas, ésta no debe haber sido modificada al menos en los 90 días previos a la selección del paciente para su participación en el estudio.
- El sujeto y su representante legal previo consentimiento informado aceptan participar en estudios genéticos de la Apolipoproteína E.
Criterios de exclusión:
- Presencia de EA en grado moderado o severo.
- Hallazgos clínicos consistentes con otras demencias degenerativas primarias (demencia con cuerpos de Lewy, demencia frontotemporal, enfermedad de Huntington, enfermedad de Creutzfeldt-Jakob, síndrome de Down, etc.), otras enfermedades neurodegenerativas (Enfermedad de Parkinson, Esclerosis Lateral Amiotrófica, etc.), enfermedades cardiovasculares y/u otras enfermedades del SNC (trauma cerebral severo, tumores, hematoma subdural, etc.)
- Presencia o antecedentes de desórdenes psiquiátricos, especialmente aquellos con síntomas positivos asociados a la EA; como agresividad, agitación o alucinaciones.
- Enfermedades sistémicas severas que puedan complicar la permanencia del sujeto en el estudio.
- Antecedentes de infarto cerebral.
- Historia clínica de convulsiones y uso de antiepilépticos.
- Historia clínica de infarto de miocardio u otras afecciones cardiovasculares severas.
- Hipertensión no controlada (sistólica > 160 mmHg and / o diastólica > 95 mmHg), hipotensión sistémica (SBP <86 mmHg) o bradicardia (<50 latidos por min).
- Fallo renal, fallo hepático y/o fallo respiratorio (necesidad de suplementación de oxígeno).
- Uso de antidepresivos, sedantes e hipnóticos en los 30 días previos al estudio.
- Tratamiento con fármacos experimentales para la EA en los 60 días previos al inicio del estudio.
2.5. Tratamiento del estudio
El medicamento se administrará de forma oral a dosis única y los brazos de tratamiento son los siguientes:
- Tratamiento con el placebo (brazo 1 - control)
- Tratamiento con Faimerol a una dosis de 60 mg/día (brazo 2 – experimental)
- Tratamiento con Faimerol a una dosis de 120 mg/día (brazo 3 – experimental)
2.6. Variables de estudio
Variables de eficacia:
- Evaluación de la memoria de trabajo en los sujetos (estado inicial vs 32 semanas y 52 semanas de estudio) mediante el test COWAT.
- Evaluación de la fluidez verbal mediante el test de fluidez verbal (estado inicial vs 24 semanas y 52 semanas de estudio).
- Evaluación de la velocidad de procesamiento mediante la prueba de comprensión, test WAIS (estado inicial vs 24 semanas y 52 semanas de estudio).
- Evaluación de cambios en las funciones ejecutivas mediante el test de dígitos (estado inicial vs 4 semanas, 16, 24, 32 y 52 semanas de estudio).
- Cambios en los biomarcadores tau y tau fosforilada en líquido cefalorraquídeo (LCR) (estado inicial vs 52 semanas).
- Evaluación de cambios sinápticos y atrofia hipocampal mediante RM (estado inicial vs 52 semanas).
Variables de seguridad:
- Evaluación de la concentración de Faimerol en plasma y LCR.
- Número de acontecimientos adversos (AA)/acontecimientos adversos graves (AAG) durante el tratamiento y 2 semanas después del cese del tratamiento (cuantificando el número de sujetos con AA/AAG y cambios en sus constantes vitales).
2.7. Metodología estadística
Estimación del tamaño muestral: en base a los estudios previos con pacientes de EA en fase II y mediante un programa estadístico que determinó las condiciones óptimas para un valor de α = 0,05 (dos colas) y una potencia del 80% (β = 0,20).
Hipótesis de estudio: Faimerol evita la progresión de los déficits cognitivos en pacientes con EA en estadio leve. Es una hipótesis de superioridad, ya que se espera que el tratamiento mejore los deficientes cognitivos en estadios leves de EA y/o evite la progresión de la enfermedad respecto al tratamiento placebo. En este ensayo clínico el uso de placebo como tratamiento control es ético ya que no hay comercializados tratamientos efectivos para la EA.
Referencias
Anand, R., R., Gill, K., & Mahdi, A. (2014). Therapeutics of Alzheimer’s disease: present and future. Neuropharmacology, 76(Part A), 27–50.
Anstey, K., Cherbuin, N., Budge, M., & Young, J. (2011). Body mass index in midlife and late-life as a risk factor for dementia: a meta-analysis of prospective studies. Obesity Rev, 12:e426–37.
Bagyinszky, E., Youn, Y., An, S., & Kim, S. (2014). The genetics of Alzheimer’s disease. Clinical Interv Aging, 9, 535–551.
Ballard, C., Gauthier, S., Corbett, A., Brayne, C., Aarsland, D., & Jones, E. (2011). Alzheimer’s disease. Lancet, 377(9770), 1019–1031., C., Gauthier, S., Corbett, A., Brayne, C., Aarsland, D., & Jones, E. (2011). Alzheimer’s disease. Lancet, 377(9770), 1019–1031.
Burns, A., & Iliffe, S. (2009). Alzheimer’s Disease. BMJ, 338:b158.
Cataldo, J., Prochaska, J., & Glantz, S. (2010). Cigarette smoking is a risk factor for Alzheimer’s disease: An analysis controlling for tobacco industry affiliation. J Alzheimer Disease, 19(2), 465–480.
Cummings, J., Lee, G., Ritter, A., Sabbagh, M., & Zhongc, K. (2019). Alzheimer’s disease drug development pipeline: 2019. Alzheimers Dement, 5, 272–293.
Folstein, M., Folstein, S., & McHugh, P. (1975). “Mini-mental State”. A Practical Method for Grading the Cognitive State of Patients for the Clinician. J Psychiatric Res, 12(3), 189–198.
Garre-Olmo, J. (2018). Epidemiología de la enfermedad de Alzheimer y otras demencias. Revista Neurología, 66, 377–386.
Guerreiro, R., & Hardy, J. (2014). Genetics of Alzheimer’s disease. Neurotherapies, 11, 732–737.
Hardy, J., Bogdanovic, N., Winblad, B., Portelius, E., Andreasen, N., Cedazo-Minguez, A., & Al, E. (2014). Pathways to Alzheimer’s disease. J Intern Med, 275(3), 296–303.
Hippius, H., & Neundorfer, G. (2003). The discovery of Alzheimer’s disease. Dialogues Clin Neurosci, 5, 101–108.
Hung, S., & Fu, W. (2017). Drug Candidates in Clinical Trials for Alzheimer’s Disease. J Biomed Sci, 24(1), 47.
Hyman, B., Phelps, C., Beach, T., & Al, E. (2012). National Institute on Aging– Alzheimer’s Association guidelines for the neuropathologic assessment of Alzheimer’s disease. Alzheimers Dement, 8, 1–13.
International Conference on Harmonisation. (2009). Guidance on nonclinical safety studies for the conduct of human clinical trials and marketing authorisation for pharmaceuticals M3(R2). Retrieved from http://www.ich.org/fileadmin/Public_Web_Site/ICH_Products/Guidelines/Multidisciplinary/M3_R2/
McKhann, G., Knopman, D., Chertkow, H., Hyman, B., Jack, C., Kawas, C., & Al., E. (2011). The Diagnosis of Dementia Due to Alzheimer’s Disease: Recommendations From the National Institute on Aging-Alzheimer’s Association Workgroups on Diagnostic Guidelines for Alzheimer’s Disease. Alzheimers Dement, 7(3), 263–269.
Méndez, M. (2012). Early-onset Alzheimer’s Disease: Nonamnestic Subtypes and Type 2 AD. Arch Med Res, 43(8), 677–685.
Moussa, C. (2017). Beta-secretase inhibitors in phase I and phase II clinical trials for Alzheimer’s disease. Expert Opinion on Drug Discovery, 26(10), 1131–1136.
Niu, H., Álvarez-Álvarez, I., Guillén-Grima, F., & Aguinaga-Ontoso, I. (2017). Prevalence and Incidence of Alzheimer’s Disease in Europe: A Meta-Analysis. Neurologia, 32(8), 523–532.
Ower, K., Hadjichrysanthou, C., Gras, L., Goudsmit, J., Anderson, R., & de Wolf, F. (2018). Temporal association patterns and dynamics of amyloid-ß and tau in Alzheimer‘s disease. Eur J Epidemiol, 33(7), 657–666.
Rosendorff, C., Beeri, M., & Silverma, J. (2007). Cardiovascular Risk Factors for Alzheimer’s Disease. The American Journal of Geriatric Cardiology, 16(3), 143–149.
Scheltens, P., Blennow, K., Breteler, M., & Al, E. (2016). Alzheimer’s disease. Lancet, 388, 505–517.Selkoe, D., & Hardy, J. (2016). The amyloid hypothesis of Alzheimer’s disease at 25 years. EMBO Mol Med, 8, 595–608.
